鲁凤民团队采用基因编辑和RNA干扰技术高效抑制HBV复制获新进展
近期,北京大学基础医学院鲁凤民教授课题组与许中伟、夏宁邵教授等合作,在《 Theranostics 》杂志上在线发表了题为“The gRNA-miRNA-gRNA ternary cassette combining CRISPR/Cas9 with RNAi approach strongly inhibits hepatitis B virus replication”的研究论文。该研究通过模拟microRNA(miRNA)的生成过程,整合双gRNA导向的CRISPR/Cas9和RNA干扰技术,高效破坏乙型肝炎病毒(HBV)的复制模板-共价闭合环状DNA(cccDNA),探索病毒清除新路径。北医王杰讲师、陈然和张瑞阳博士研究生为该论文的共同第一作者。
目前,我国仍有慢性HBV感染者约7800万人,慢乙肝患者约2800万人。HBV感染仍是我国病毒性肝炎、肝硬化及肝癌的重要致病因素。作为HBV复制模板的cccDNA,由于其半衰期相对较长,加上cccDNA池的不断补充,使得细胞核内的cccDNA持续存在、感染慢性化。目前,临床上治疗慢乙肝的常用药物为核苷(酸)类似物和长效干扰素,二者均不直接作用于cccDNA,难以有效清除病毒实现临床治愈。因此,研发直接靶向cccDNA的药物,寻找清除cccDNA的新方法和新策略,是当前慢乙肝治疗药物研发的热点。
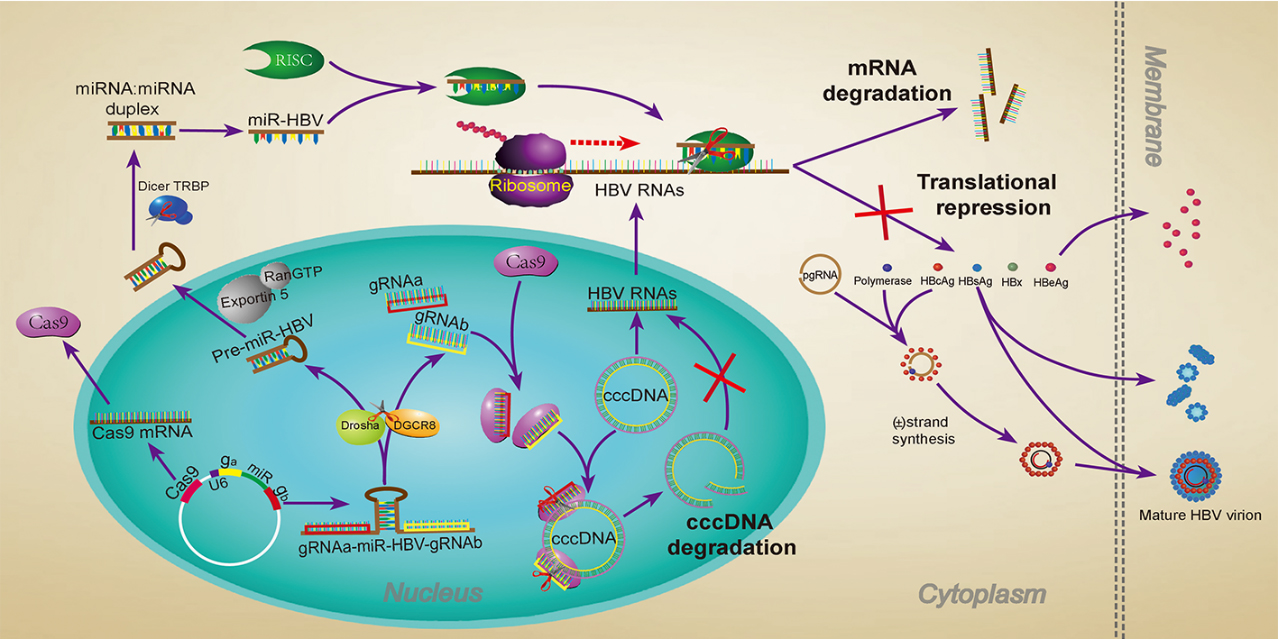
双gRNA导向的CRISPR/Cas9整合RNAi技术高效抑制HBV复制模式图
该研究以miRNA-31为基本骨架,通过模拟其核心序列的二级结构设计HBV特异的miRNA(miR-HBV),miRNA两侧侧翼序列为特异性靶向cccDNA不同位点的引导RNA(gRNA)。如图所示,该gRNA-(miR-HBV)-gRNA三联体表达体系导入细胞后,在细胞核内转录形成gRNA-(miR-HBV)-gRNA长转录本,经内源的Drosha/DGCR8复合体剪切,形成2个gRNA和1个miR-HBV前体(pre-miR-HBV)。进入细胞质后,pre-miR-HBV 进一步经Dicer酶剪切,形成成熟的miR-HBV。一方面双gRNA导向的CRISPR/Cas9系统通过切割并去除cccDNA的关键调控和编码序列直接破坏cccDNA,另一方面通过miR-HBV在转录后水平抑制HBV复制,进而抑制cccDNA池的补充,协同促进HBV cccDNA的清除。此外,本研究还发现,当pri-miRNA-31的侧翼序列长度为38 bp时与双gRNA组成的三联体对HBV复制的抑制效率最高。
当然,该技术离临床应用尚有较远的距离。一方面如何高效和靶向性地将三联体递送到HBV感染的肝细胞内是需要攻克的一大障碍;另一方面,CRISPR/Cas9基因编辑技术的脱靶效应也有安全性之虞。然而,近年来随着Cas核酸酶的不断改造,其脱靶效应得到了有效控制,安全性大为提高。而且,随着金黄色葡萄球菌Cas9的发现,使得CRISPR/Cas9系统可以装入腺相关病毒载体中,致使该技术应用于临床的距离逐渐缩短。
总之,本研究通过gRNA-(miR-HBV)-gRNA三联表达框架联合CRISPR/Cas9和RNA干扰技术高效破坏cccDNA,促进HBV清除,为慢乙肝抗病毒治疗提供了新的思路。该项研究得到国家十二五重大科技专项计划“艾滋病和病毒性肝炎等重大传染病防治”项目和国家自然科学基金的支持。
论文链接:https://www.ncbi.nlm.nih.gov/pubmed/28839466
(基础医学院)
编辑:韩娜


