基础医学院王娟团队揭示肠道菌群参与孤独症发病新机制
近日,北京大学基础医学院医学生物信息学系王娟团队与中科院北京基因组所康禹团队合作在Science Advances杂志发表了文章A quasi-paired cohort strategy reveals the impaired detoxifying function of microbes in the gut of autistic children。他们应用宏基因组学技术,采用类配对分析方法,揭示了孤独症患者肠道菌群失衡,解毒功能障碍,进而导致患者机体毒素蓄积和线粒体功能障碍。孤独症儿童肠道菌群代谢功能的改变可能参与孤独症发病机制。这个发现可能为未来孤独症干预提供新的策略。

孤独症谱系障碍(Autism Spectrum Disorder,ASD)是一组复杂的神经发育障碍性疾病,主要特征为受损的社交功能,重复刻板行为,狭窄兴趣。在世界范围内,孤独症的发病率逐渐攀升,美国疾病预防中心今年发布的美国8岁儿童的孤独症患病率为1/54,孤独症发病率呈现持续上升的趋势。目前,孤独症的病因仍然不清楚,环境因素和遗传因素的交互作用可能导致疾病发生。最近很多研究显示肠道菌群在孤独症中起到重要作用。由于胃肠道共患病在孤独症儿童中非常普遍。同时孤独症儿童非常挑食且体内缺乏某些消化酶,这不可避免地改变了营养物质和菌群代谢物的水平,对共生菌的定植产生影响,导致了菌群失调。另外,很多研究发现了孤独症儿童肠道菌群失调,比如双歧杆菌丰度降低,梭菌属丰度上升,肠道菌群失调被认为与肠道黏膜炎症以及肠道通透性增加相关。
基于鸟枪法测序的宏基因组学研究被广泛应用于探索微生物与宿主之间的关系,也被用于寻找微生物参与的疾病发病因素。宏基因组测序提供了更高的物种分辨率以及更全面的微生物功能信息。但是,肠道微生物受多种因素影响,比如遗传、年龄、饮食和健康等等,即使在健康人群中微生物组也存在极大的异质性。此外,肠道微生物组分被复杂的代谢网络所限制。基于这些因素,王娟团队开发了一种新型的宏基因组分析策略,即类配对分析法,将具有相似代谢背景的孤独症组和对照组个体一一配对,将原始的分组转换为边界配对组。这种分析方法类似于基因组分析中的双胞胎研究。这样不仅降低了个体异质性,而且增加了统计功效。
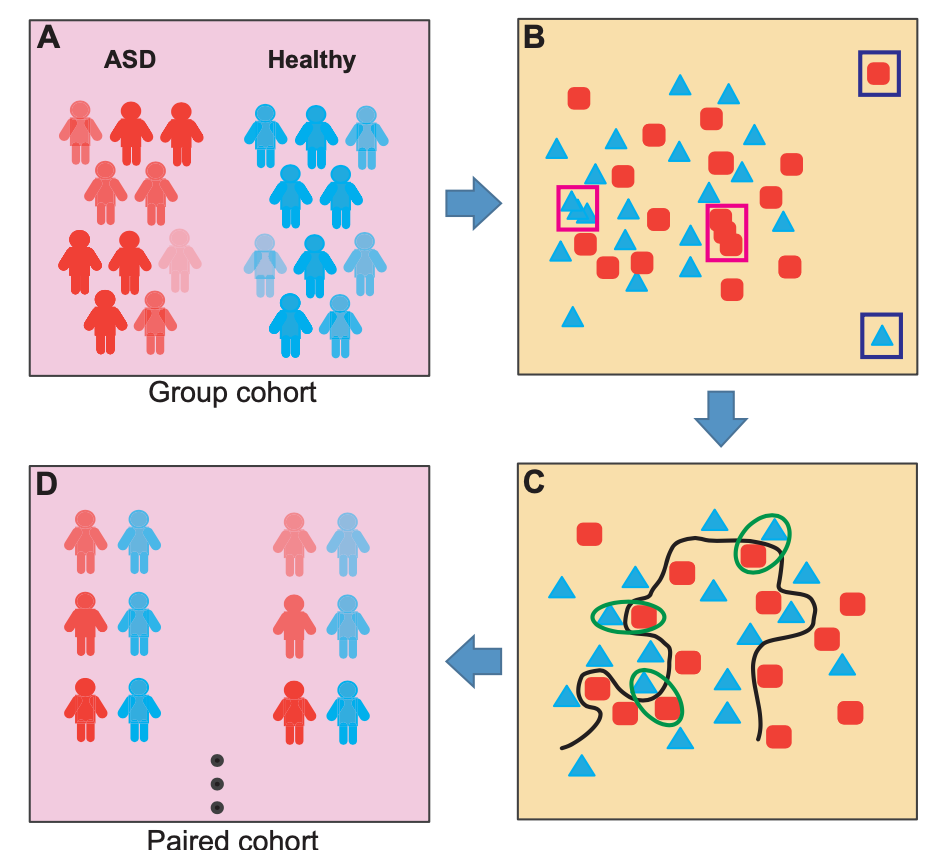
他们对79份来自于孤独症组和对照组的样本进行了宏基因组测序,并且对测序得到的数据运用了类配对分析策略,以鉴定孤独症相关的菌群代谢通路。分析发现孤独症儿童肠道菌群在解毒的酶和通路方面有明显缺陷,主要涉及谷胱甘肽(关键的抗氧化剂和解毒酶辅因子)生成和有机毒素降解。这些解毒酶的丰度与线粒体功能紊乱标志物负相关,提示菌群解毒功能对线粒体有潜在保护作用。基于这些酶的的诊断模型能准确区分孤独症儿童与健康对照儿童(AUC 0.88),且诊断分数与孤独症临床评分相关。流行病学研究发现环境毒素暴露是孤独症的重要环境因素,孤独症儿童肠道解毒功能受损解释了患者对毒素暴露更敏感的原因。该研究发现了微生物参与孤独症发病的重要新机制,并为孤独症医学干预提供新的策略。

北京大学基础医学院2015级硕士研究生张梦想、中科院基因组所楚亚男博士和硕士研究生孟庆仁为论文共同第一作者。
原文链接:
https://advances.sciencemag.org/content/6/43/eaba3760
王娟,2005年毕业于中国协和医科大学,获得医学博士学位;2005-2011年在北京大学医学部基础医学院医学生物信息学系任讲师,2011年任副教授,同时担任北京大学医学部孤独症研究中心秘书长,长期从事孤独症系统生物医学研究,已在ScienceAdvances、NucleicAcidsResearch、 Trends in Molecular Medicine、 BriefingsinBioinformatics、 Scientific Reports、Frontiers in Genetics发表多篇论文。

左一为硕士研究生何一,左二为王娟,左三为硕士研究生张梦想(本文第一作者)

王娟
(基础医学院)
编辑:玉洁


