科技创新助推高质量发展 北医三院多项科技成果发表(4)
2022年,北京大学第三医院(以下简称“北医三院”)成为公立医院高质量发展试点医院。围绕科技创新工作,北医三院通过平台搭建、资源配置、经费支持等多方面举措,为全院开展创新工作搭建了广阔的舞台,创造了科技发展新生态。各研究团队积极探索,创新能力明显提升,取得了多项科研成果。
本期主要包括4篇优秀论文成果:
1 普通外科、肿瘤中心付卫团队与北京大学生物医学前沿创新中心汤富酬团队合作在Cell Discovery期刊发表的关于“解析小肠癌分子特征和肿瘤微环境”的研究成果;
2 药剂科林坚研究员、陈龙副研究员临床药学分子交叉团队与合作者在Signal Transduction and Targeted Therapy期刊发表的关于“发现打开血迷路屏障的全新靶点”的研究成果;
3 运动医学科敖英芳教授、胡晓青研究员团队与北京化工大学蔡晴教授团队合作在Advanced Functional Materials期刊发表的关于“开发了一种3D 生物打印新型动态结构水凝胶,促进异质性骨软骨缺损修复再生”的研究成果;
4消化科丁士刚教授团队与北京大学基础医学院陈香梅副教授、鲁凤民教授团队在Emerging Microbes & Infections期刊发表的关于“发现单纯HBsAg宫内暴露增强了子代小鼠抗原特异性免疫应答从而促进了HBV的清除”的研究成果;
付卫、汤富酬团队解析小肠癌分子特征和肿瘤微环境
2022年9月14日,北医三院普通外科、肿瘤中心付卫教授团队与北京大学生物医学前沿创新中心汤富酬教授团队合作,在Cell Biology(细胞生物学)领域排名第七的Cell Discovery期刊发表题为“Single-cell profiling reveals molecular basis of malignant phenotypes and tumor microenvironments in small bowel adenocarcinomas”针对小肠癌的研究成果。
该研究利用单细胞转录组测序技术对12例小肠癌组织进行分析,系统地揭示了小肠癌肿瘤细胞和肿瘤微环境细胞的分子特征,比较了小肠癌与其他消化道恶性肿瘤在转录组水平的差异,在此基础上利用小肠癌的基因表达特点预测了一批治疗小肠癌的潜在候选药物并且进行了体外验证。该项工作揭示了小肠癌的重要分子特征,同时为小肠癌的临床治疗提供了重要的线索和理论依据。

北医三院普通外科周鑫副研究员、王文东、路永衢博士,北京大学生物医学前沿创新中心杨经纬、董骥博士为文章的共同第一作者。付卫教授和汤富酬教授为文章的共同通讯作者。本研究获得国家自然科学基金委员会和北京未来基因诊断高精尖创新中心的资助。
全文链接:https://www.nature.com/articles/s41421-022-00434-x
药剂科林坚研究员、陈龙副研究员临床药学分子交叉团队与合作者发现打开血迷路屏障的全新靶点
2022年6月10日,北医三院药剂科林坚研究员、陈龙副研究员临床药学分子交叉团队与合作者在Biochemistry & Molecular Biology(生物化学与分子生物学)领域排名第四的Signal Transduction and Targeted Therapy期刊发表题为“LDL receptor-related protein 1 (LRP1), a novel target for opening the blood-labyrinth barrier (BLB)”的研究成果,首次展示了全新的打开血迷路屏障的靶点:低密度脂蛋白受体相关蛋白1(LRP1),并通过此靶点在国际上首次实现了系统性、无创性的跨越血迷路屏障递送药物,为内耳相关疾病的无创诊疗提供了全新的靶点和工具。
中国每年受内耳相关疾病困扰的患者高达数千万人,而血迷路屏障的存在极大的限制患者的临床获益,发展系统性、无创性的内耳药物递送是领域内亟待解决的难题。论文中,作者由生物信息学分析出发,首次发现了与血迷路屏障密切相关的靶点:LRP1,并通过高通量筛选的方法获得了结合LRP1的多肽配体:IETP2。通过LRP1介导的转运,可以将IETP2无创性的递送到小鼠和猪的内耳部位,并因此实现了内耳诊疗药物的系统性、无创性内耳递送。
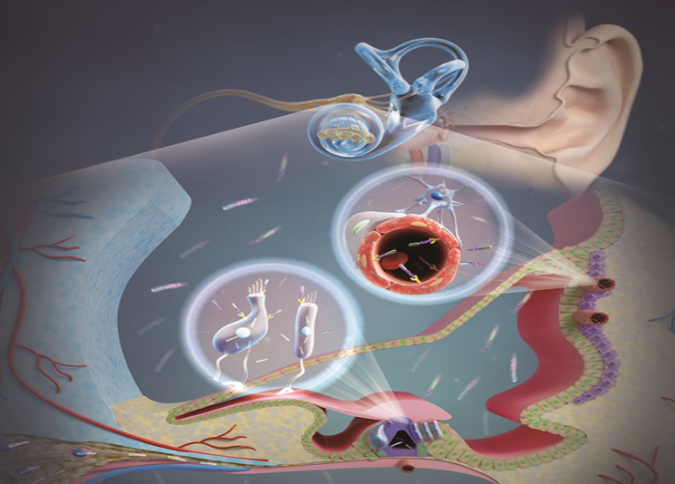
打开血迷路屏障的全新靶点和无创药物递送系统
北医三院药剂科陈龙副研究员为文章的共同第一作者,药剂科林坚研究员为文章的共同通讯作者。本研究获得国家自然科学基金、国家重点研发计划、国家科技重大专项的资助。
全文链接:https://www.nature.com/articles/s41392-022-00995-z
运动医学科敖英芳教授、胡晓青研究员团队与北京化工大学蔡晴教授团队合作开发了一种3D 生物打印新型动态结构水凝胶,促进异质性骨软骨缺损修复再生
2022年2月,北医三院运动医学科敖英芳教授、胡晓青研究员课题组与北京化工大学蔡晴教授课题组在Physics, Applied(应用物理学)领域排名第八的Advanced Functional Materials期刊发表题为“3D Bioprinting of Heterogeneous Constructs Providing Tissue-Specific Microenvironment Based on Host–Guest Modulated Dynamic Hydrogel Bioink for Osteochondral Regeneration”的研究成果。本研究对新型生物墨水进行探索,提出了基于主客体相互作用构建多功能生物墨水的新策略,突破了传统生物墨水难以仿生构建具有复杂结构的组织的应用瓶颈。
在本研究中,利用主客体相互作用形成动态网络,构建具有增强的细胞适应性、良好的细胞粘附性、增强的机械性能以及可调的模量的新型生物墨水。此外,基于超分子结构提供的持续药物缓释能力,将kartogenin(一种促进软骨形成的小分子药物)用于具有较低杨氏模量的上层软骨区域,并将褪黑素(一种促进骨形成的小分子药物) 用于具有较高杨氏模量的下层软骨下骨区域,以模拟具有生物化学以及生物力学双相梯度的异质性骨软骨微环境,实现软骨和软骨下骨的同时再生。
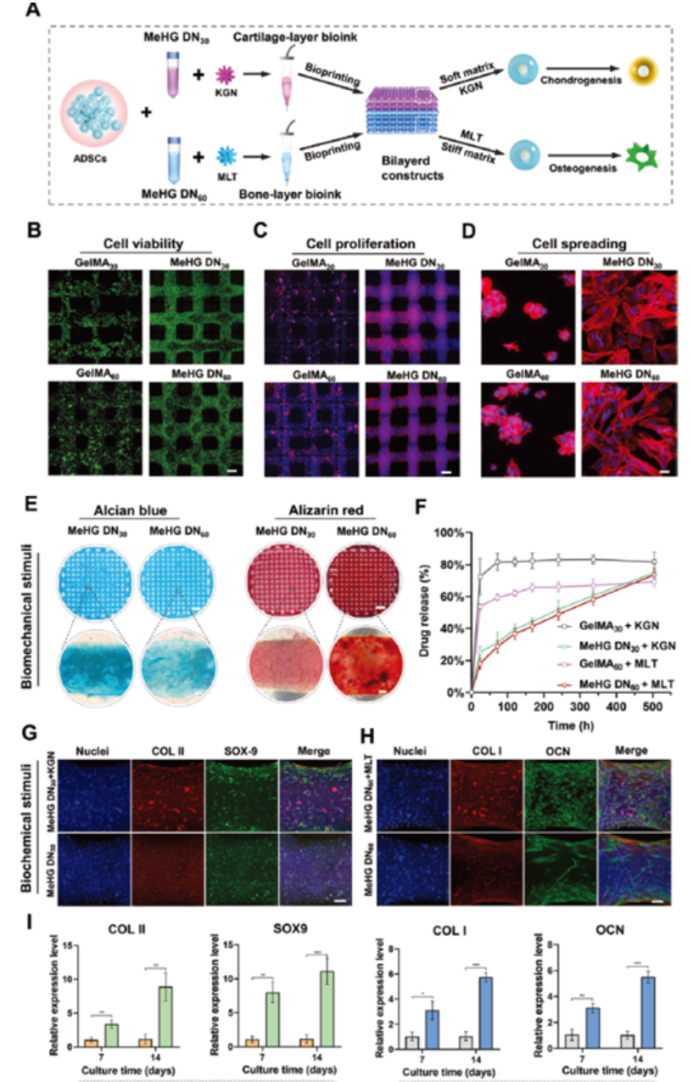
基于新型生物墨水3D 生物打印的干细胞共培养结构
表现出优异的细胞活力、增殖、适应以及成软骨和成骨分化能力
北医三院运动医学科代文立博士、浙江大学材料学院张枥文博士为文章的共同第一作者,北医三院运动医学科敖英芳教授、胡晓青研究员与北京化工大学材料学院蔡晴教授为文章的共同通讯作者。本研究获得国家重点研发计划“科技冬奥”重点专项、国家自然科学基金的资助。
全文链接:https://onlinelibrary.wiley.com/doi/10.1002/adfm.202200710
丁士刚教授团队与北京大学基础医学院陈香梅副教授、鲁凤民教授团队发现单纯HBsAg宫内暴露增强了子代小鼠抗原特异性免疫应答从而促进了HBV的清除
2022年5月,北医三院丁士刚教授团队与北京大学基础医学院陈香梅副教授、鲁凤民教授团队在Microbiology(微生物学)领域排名第七的Emerging Microbes & Infections期刊发表题为“Solely HBsAg intrauterine exposure accelerates HBV clearance by promoting HBs-specific immune response in the mouse pups”的研究成果。发现了有关乙型肝炎病毒表面抗原(HBsAg)宫内暴露对于子代免疫应答影响的新机制。
慢性乙型肝炎病毒(HBV)感染是我国肝硬化、肝细胞癌及严重终末期肝病发生的主要原因,严重危害国人健康。而HBV慢性感染主要发生在围生期,因此预防和阻断母婴传播对减少甚至消除我国的HBV感染流行具有重要意义。该研究通过使用单纯HBsAg宫内暴露小鼠模型研究了HBsAg宫内暴露对HBV持续复制的影响和潜在机制。当HBsAg宫内暴露小鼠在出生后通过尾静脉水压动力注射方式再次暴露于HBV时,这些小鼠的HBV清除显著增快,HBsAg特异性CD8+ T细胞显著增多,同时小鼠肝脏中的IFN-γ分泌增加。机制上,HBsAg宫内暴露可激活抗原呈递细胞——树突状细胞,增强对HBsAg的递呈能力从而产生抗原特异性T细胞免疫记忆。这项研究为HBsAg宫内暴露激活了新生儿免疫应答提供了重要的实验证据。

北医三院消化科博士后宁静和首都医科大学附属北京儿童医院王建文博士为文章的共同第一作者。北京大学基础医学院陈香梅副教授、鲁凤民教授和北医三院消化科丁士刚教授为文章的共同通讯作者。本研究获得“十三五”国家科技重大专项及国家自然科学基金的资助。
全文链接:https://www.tandfonline.com/doi/full/10.1080/22221751.2022.2071172
(北医三院)
编辑:玉洁


