北京大学第三医院洪天配/魏蕊团队在Metabolism发表最新研究成果 发现胰岛功能调控新机制
2024年10月1日,北京大学第三医院内分泌科洪天配教授/魏蕊研究员团队在内分泌代谢专业传统优秀期刊《代谢》(Metabolism)在线发表胰岛功能调控的最新研究成果。论文题目为:《α细胞Fam3a介导的激素原转化酶更替可呈Nr4a2-Foxa2依赖性方式调控胰岛GLP-1产生》(Fam3a-mediated prohormone convertase switch in α-cells regulates pancreatic GLP-1 production in an Nr4a2-Foxa2-dependent manner)。

论文截图
序列相似性家族3成员A(Family with sequence similarity 3 member A,Fam3a)是新近发现的一种线粒体蛋白,参与糖尿病、代谢相关脂肪性肝病等代谢性疾病的发生发展。
既往研究表明,Fam3a促进胰岛β细胞合成和分泌胰岛素,增强β细胞功能,改善糖尿病小鼠的血糖水平。然而,Fam3a在胰岛其他类型细胞中的作用,迄今未见报道。
本课题组和其他团队的研究证实,胰岛β细胞特异性敲除Fam3a的小鼠随着年龄增长而出现高血糖表型,而全身敲除Fam3a小鼠则无明显的糖耐量异常。上述结果提示,其他类型胰岛细胞Fam3a缺失可能在维持血糖稳态中发挥有益作用,从而抵消β细胞Fam3a缺失导致的糖代谢紊乱。
在胰岛组织中,α细胞占比仅次于β细胞。因此,本研究聚焦于胰岛α细胞,旨在阐明Fam3a在α细胞中的作用。胰岛α细胞主要分泌胰高糖素,与β细胞分泌的胰岛素共同调节机体血糖稳态。近年来,本课题组和其他团队的研究均证实,α细胞还可分泌胰高糖素样肽-1(GLP-1),并且参与调控机体葡萄糖代谢。
本研究的主要成果如下:
动物实验显示,在全身敲除Fam3a的小鼠中,α细胞GLP-1产生显著增加。其次,利用人类胰岛单细胞测序和转录组测序的数据库分析证实,人类α细胞中FAM3A与PCSK1(编码PC1/3,一种可将胰高糖素原剪切加工为活性GLP-1的关键酶)表达水平之间呈负相关,提示FAM3A下调可能促进人类α细胞产生GLP-1。
本研究通过构建胰岛α细胞特异性Fam3a敲除小鼠开展系列动物实验。结果显示,无论是在正常生理条件下,还是在高脂饮食和糖尿病两种代谢应激模型中,α细胞Fam3a缺失均可上调胰岛来源的GLP-1、提高血浆胰岛素水平。进一步添加GLP-1受体拮抗剂证实,α细胞来源的GLP-1通过旁分泌作用促进β细胞分泌胰岛素,进而在正常生理条件和代谢应激状态下改善葡萄糖代谢。
为探究Fam3a缺失促进α细胞产生GLP-1的机制,本研究在胰岛α细胞中利用Fam3a基因过表达或敲减实验、转录组测序、免疫共沉淀、核转位检测、基因截短或点突变技术、双荧光素酶报告基因分析等一系列体外实验证实,Fam3a通过上调Nr4a2促进Foxa2核转位,Nr4a2与Foxa2两者形成蛋白复合体,作用于Pcsk1启动子的特定结合位点,从而抑制Pcsk1的转录活性。上述结果提示,在胰岛α细胞中,Fam3a通过Nr4a2-Foxa2-PC1/3轴调控α细胞来源的GLP-1产生。
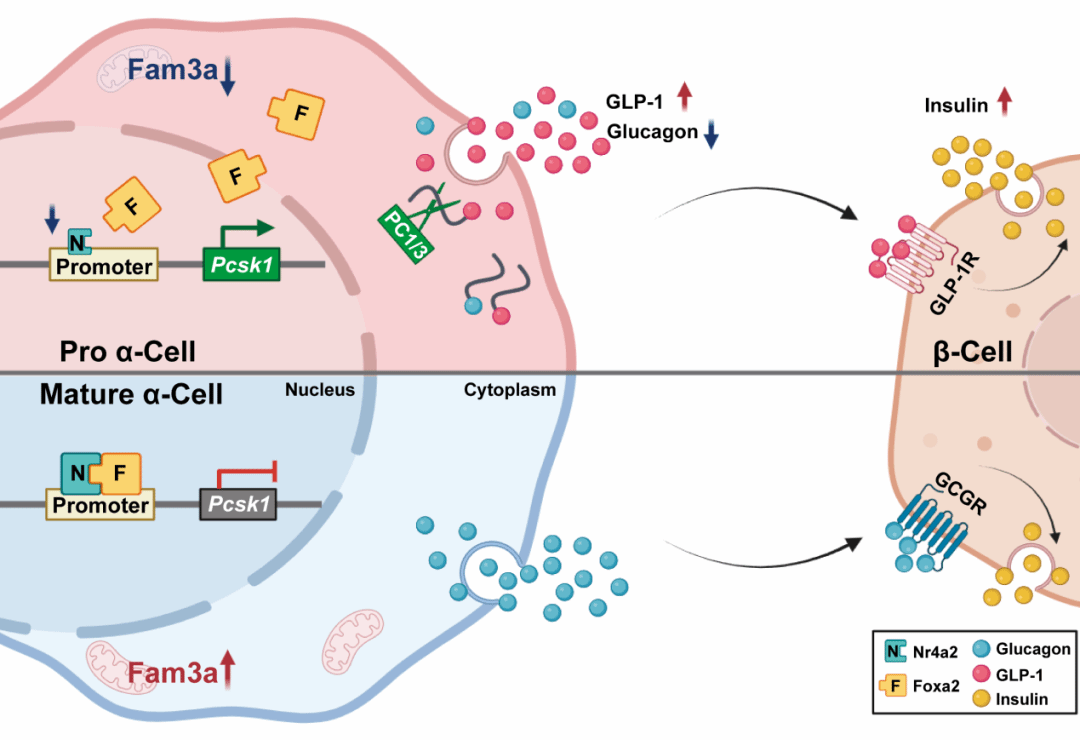
胰岛α细胞Fam3a介导的激素原转化酶更替可呈Nr4a2-Foxa2依赖性方式调控胰岛GLP-1产生的模式图
本研究首次证实胰岛α细胞Fam3a缺失可通过Nr4a2-Foxa2-PC1/3轴促进α细胞产生GLP-1,进而以旁分泌方式改善β细胞功能。
本研究成果凸显了α细胞与β细胞之间对话在维持机体血糖稳态中的重要作用,为研发靶向α细胞的糖尿病治疗策略提供新思路。

Fam3a在胰岛α和β细胞中发挥不同作用的模式图
北京大学第三医院内分泌科王丹丹博士和魏天娇博士为共同第一作者,洪天配教授和魏蕊研究员为共同通讯作者。本研究得到国家科技重大专项、国家自然科学基金等课题经费的支持。
Metabolism自1952年创刊以来,在代谢调控与代谢性疾病研究领域一直具有非常高的影响力,是内分泌代谢专业排名前5%的期刊。
北京大学第三医院内分泌科洪天配/魏蕊团队长期致力于胰岛再生和β细胞功能调控研究,近五年,在Diabetologia(封面文章)、Diabetes(封面和Highlight文章各1篇)、Metabolism(2篇)、Lancet子刊EBioMedicine(配发同期述评)、Cell子刊iScience(2篇)、Diabetes Metab Res Rev(封面文章)等SCI期刊发表相关论著近20篇。
原文链接:https://doi.org/10.1016/j.metabol.2024.156042
【延伸阅读】
作者介绍
共同第一作者
王丹丹

北京大学第三医院内分泌科2024届博士毕业生
魏天娇

北京大学第三医院内分泌科2023级博士研究生
内分泌科主管技师
共同通讯作者
魏蕊

北京大学第三医院内分泌科研究员
博士生导师、博士后合作导师
主要研究方向:胰岛再生及糖尿病治疗新靶点
洪天配

北京大学第三医院内分泌科主任
教授、主任医师、博士生导师
主要研究方向:糖尿病基础与临床研究、干细胞分化研究等
参考文献:
1. Yang W, Chi Y, Meng Y, Chen Z, Xiang R, Yan H, et al. FAM3A plays crucial roles in controlling PDX1 and insulin expressions in pancreatic beta cells. FASEB J 2020;34:3915–31. https://doi.org/10.1096/fj.201902368RR.
2. Wei R, Cui X, Feng J, Gu L, Lang S, Wei T, et al. Dapagliflozin promotes beta cell regeneration by inducing pancreatic endocrine cell phenotype conversion in type 2 diabetic mice. Metabolism 2020;111:154324. https://doi.org/10.1016/j.metabol.2020.154324.
3. Wei T, Cui X, Jiang Y, Wang K, Wang D, Li F, et al. Glucagon acting at the GLP-1 receptor contributes to β-cell regeneration induced by glucagon receptor antagonism in diabetic mice. Diabetes 2023;72:599–610. https://doi.org/10.2337/db22-0784.
4. Campbell SA, Golec DP, Hubert M, Johnson J, Salamon N, Barr A, et al. Human islets contain a subpopulation of glucagon-like peptide-1 secreting α cells that is increased in type 2 diabetes. Mol Metab 2020;39:101014. https://doi.org/10.1016/j.molmet.2020.101014.
5. Ellingsgaard H, Hauselmann I, Schuler B, Habib AM, Baggio LL, Meier DT, et al. Interleukin-6 enhances insulin secretion by increasing glucagon-like peptide-1 secretion from L cells and alpha cells. Nat Med 2011;17:1481–9. https://doi.org/10.1038/nm.2513.
(北医三院)
编辑:玉洁


