新突破!北大医院薛晴教授团队发现新型纳米颗粒助力子宫内膜异位症治疗
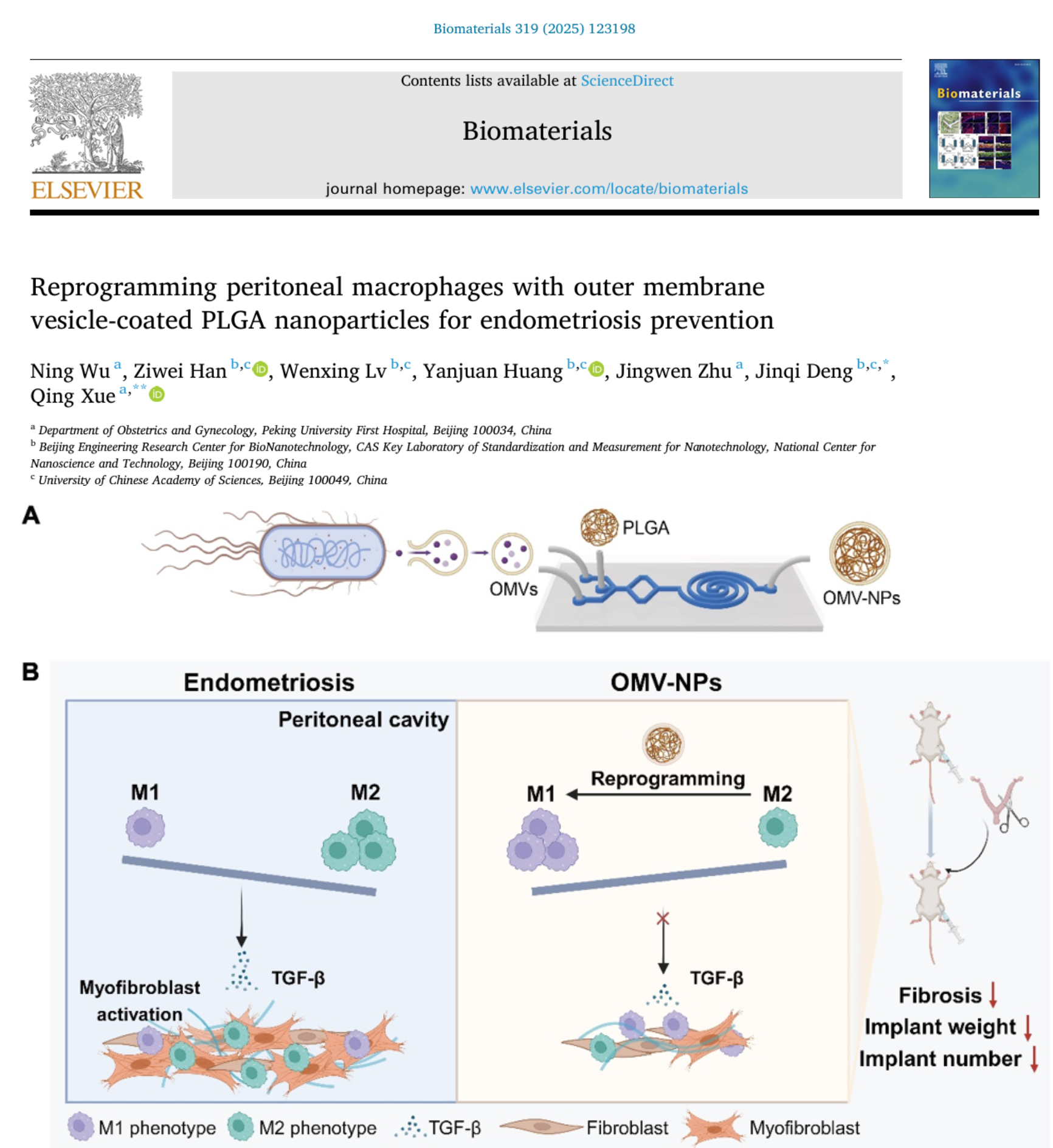
在最新发表于国际知名杂志《Biomaterials》(2023 年影响因子 12.8,Q1)的研究中,薛晴教授团队开发了一种新型的纳米治疗策略——外膜囊泡(OMV)包被的聚乳酸 - 羟基乙酸共聚物(PLGA)纳米颗粒(OMV-NPs),用于治疗子宫内膜异位症。该研究由薛晴教授指导,其博士生伍宁作为第一作者,国家纳米科学中心孙佳姝团队的邓瑾琦研究员为共同通讯作者。这一成果为子宫内膜异位症的治疗提供了新的思路和方法。
研究背景
子宫内膜异位症(Endometriosis)是一种常见的慢性炎症性疾病,主要影响育龄期女性,全球约有10%的育龄妇女受其困扰。这种疾病不仅会导致盆腔疼痛、痛经和不孕,还可能严重影响患者的生活质量。目前的治疗手段主要依赖于激素疗法,但这些方法往往伴随着显著的副作用,如抑制排卵、更年期症状和骨质疏松风险。此外,手术治疗虽然常用,但复发率高,且可能损害卵巢储备。因此,开发非激素类的替代疗法已成为学界的迫切需求。
OMV-NPs的作用机制
OMV-NPs的核心是利用细菌外膜囊泡(OMVs)的免疫刺激特性。OMVs能够激活巨噬细胞,促使其分泌促炎细胞因子,并将巨噬细胞极化为M1表型。
在此项研究中,OMV-NPs被证实能够被巨噬细胞更高效地摄取,其在腹腔内的保留时间也较长,近80%的腹腔巨噬细胞能够摄取这些颗粒。这种免疫调节作用不仅改变了腹腔内的免疫微环境,还显著降低了转化生长因子-β1(TGF-β1)的产生,并抑制了肌成纤维细胞的激活。
实验结果
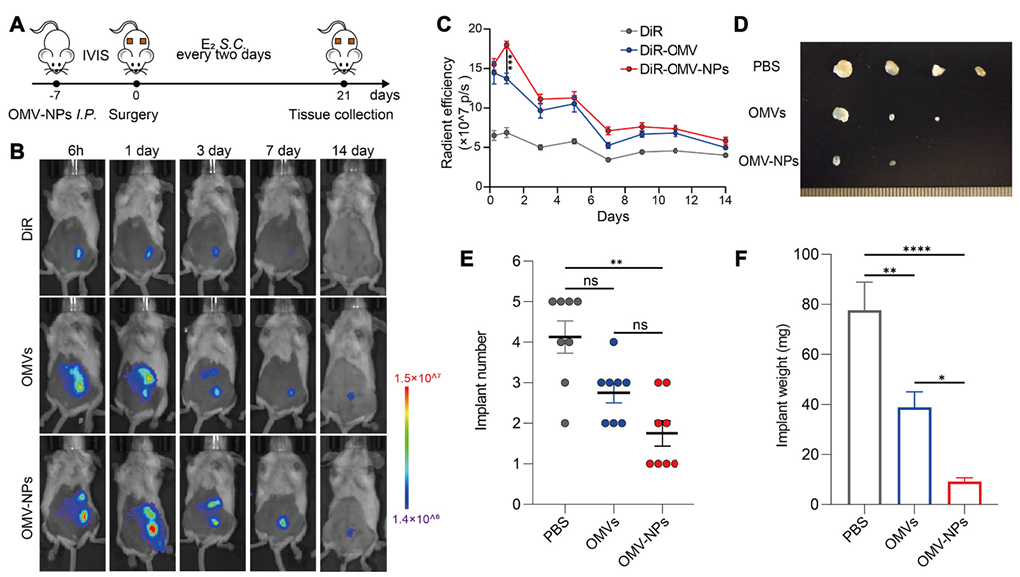
在小鼠模型中,OMV-NPs治疗显著减少了子宫内膜异位症病灶的数量和重量,同时降低了病灶内的纤维化程度。此外,通过免疫组化技术,我们发现M2极化巨噬细胞与纤维化之间存在正相关关系,这进一步证实了OMV-NPs通过重新编程巨噬细胞来抑制子宫内膜异位症进展的潜力。
临床意义与未来展望
子宫内膜异位症的治疗一直面临挑战,尤其是对于希望怀孕的女性来说,激素疗法并非理想选择。OMV-NPs作为一种非激素类的免疫疗法,为这种疾病的治疗提供了新的思路。这种纳米颗粒不仅能够精准靶向巨噬细胞,还能通过调节免疫微环境来抑制病灶的形成和发展。然而,我们的研究也存在一些局限性。例如,OMV-NPs可能在高剂量下引发系统性免疫过度激活,因此需要进一步优化剂量或通过工程化方法提高其安全性。此外,OMVs的成分复杂,未来研究需要进一步明确哪些成分对治疗效果起关键作用。尽管如此,OMV-NPs的开发为子宫内膜异位症的治疗带来了新的希望。这种纳米颗粒不仅在动物模型中显示出良好的生物相容性和安全性,还为临床应用提供了理论基础。未来,我们期待通过更多的临床前研究和临床试验,将这一创新疗法转化为实际的治疗手段,为子宫内膜异位症患者带来福音。
【延伸阅读】
第一作者

伍宁
北京大学第一医院妇产科博士研究生在读,师从薛晴教授,主要研究方向为子宫内膜异位症及卵巢功能早衰。以第一作者发表SCI及核心期刊论文4篇,其中SCI论著2篇。
通讯作者

薛晴
教授,主任医师,博士生导师,博士后合作导师
北京大学第一医院生殖医学中心主任
美国西北大学(Northwestern University)博士后
中华预防医学会生育力保护分会常务委员兼秘书长
中国医师协会生殖专业委员会委员
中国医疗保健国际交流促进会生殖医学分会常务委员
北京慢性病防治与健康教育研究会生殖医学专委会副主任委员
中国医药教育协会妇科专业委员会常务委员
中国研究型医院学会妇产科学专业委员会常务委员
国家辅助生殖技术管理专家库成员
美国生殖研究学会委员
薛晴教授近年来承担“十三五”及十四五子课题2项、国自然面上项目5项等共计10项国家级和省部级基金,以及5项校院级基金。获得北京市科技进步奖三等奖、全国妇幼健康科学技术奖二等奖等3项省部级奖项,以及国家卫健委医学科技创新大赛铜奖。在“荣耀医者”2024年度论坛荣获“生殖专科精英”称号。获得专利1项,以第一和责任作者共发表SCI论著31篇。14次参加国际大会并受邀进行口头发言,2次获得国际奖项。担任《妇科与生殖内分泌掌中宝》主编,《生育力保存的原则与实践》副主译,参与编写内异症和不孕等4项指南。
(北大医院)
编辑:玉洁


