北京大学人民医院“结直肠癌外科关键技术与个体化诊疗体系的建立及推广应用”项目荣获北京医学科技奖一等奖
2026年4月,北京医学科技奖奖励项目公布,北京大学人民医院胃肠外科团队“结直肠癌外科关键技术与个体化诊疗体系的建立及推广应用”项目荣获北京医学科技奖一等奖。项目主要完成人包括申占龙、叶颖江、王杉、高志冬、王嘉东、刘万里、姜可伟、肖毅、步召德、李昂、沈凯、王超、王搏、蒋洪朋、李晨。
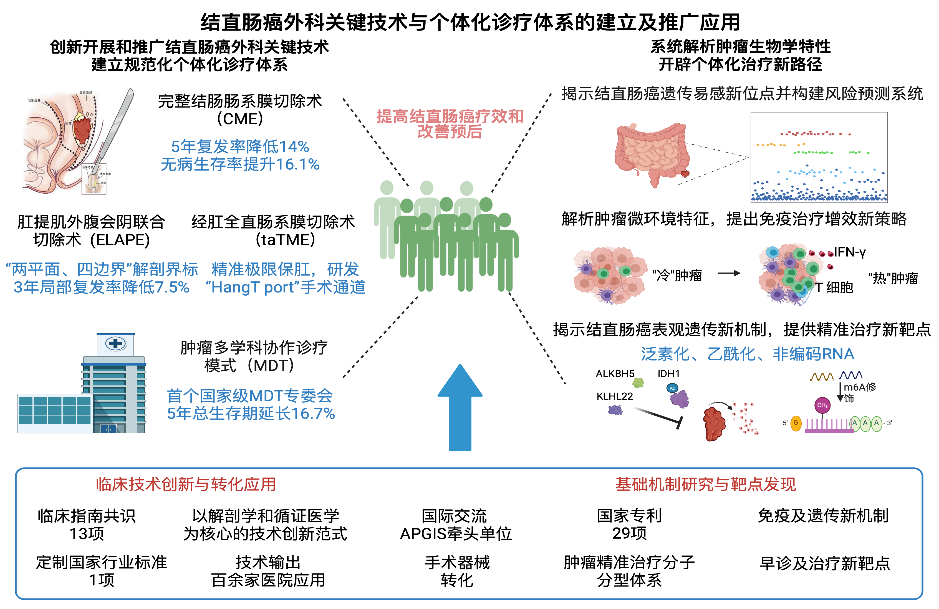
项目介绍
这不仅是一项学术荣誉,更是一次对结直肠癌诊疗格局的彻底颠覆。胃肠外科团队用20余年深耕和硬核数据证明,通过精准外科与个体化诊疗,曾经的“绝症”正加速向“慢病”转变。
毫厘之间的技术革命跨越20年时光
传统手术后仍有相当比例的患者出现局部复发或远处转移,其根源往往在于手术只切除了肿瘤本身,却留下了潜藏癌细胞的土壤——肠系膜。在胚胎发育过程中,结肠及其系膜被完整筋膜包裹,而这成为癌细胞转移的最常规路径。20年前,叶颖江与王杉两位主任医师便敏锐地捕捉到了肿瘤转移“系膜依赖性”的价值。
胃肠外科团队经过多年临床探索,率先在国内确立了“完整结肠肠系膜切除术”(CME)的手术路径——沿着两层胚胎性筋膜之间的天然间隙精准分离,将肿瘤及其潜在的转移路径整体切除,像连根带土地拔除杂草一样。
大样本临床研究证实,与传统手术相比,完整系膜切除术实现了根治更彻底、复发率大幅下降、功能保护更优这3项关键突破。这一技术将患者的5年复发率降低了14%,无病生存率提升16.1%。
基于此,胃肠外科团队开始攻克下一个难题:低位直肠癌“保命还是保肛”?胃肠外科团队创新应用经肛全直肠系膜切除术(taTME)将外科手术的“微创化”与“精准化”推向极限,对距肛缘3cm的肥胖、骨盆狭小的超低位直肠癌患者实现成功保肛。对于更棘手的经过术前临床分期评估不具备保肛条件的低位直肠癌,团队创新开展肛提肌外腹会阴联合切除术(ELAPE),通过改变传统手术入路,增加了直肠肿瘤的根治性,将3年局部复发率降低了7.5%。
MDT“集团作战”让“不可能”成为“可能”
结直肠癌肝转移曾是公认的“死亡地带”。80%—90%的肝转移患者因无法手术,5年生存率极低。从1998年开始,王杉和叶颖江带领团队打破了传统单兵作战的局限,在国内最早开启了胃肠道肿瘤MDT(多学科综合诊治)模式。这种前瞻性的“集团军作战”模式,彻底终结了患者“确诊后不知该挂哪个科”“各科室治疗方案相互矛盾”的奔波与迷茫。作为中国医师协会MDT专委会的主委单位和中国肿瘤MDT联盟的牵头单位,该模式不仅成为全国推广的规范化模板,更在实践中交出了硬核答卷——数据显示,经由这一多学科协作诊疗模式诊治的患者,5年总生存期延长了16.7%,真正实现了“1+1>2”的生命协同效应。
肿瘤生物学特性解析开辟个体化治疗新路径
近年来,免疫治疗的出现曾带来希望,但对多数结直肠癌患者却收效甚微。面对这一困境,团队联合北京大学生命科学学院、基础医学院以及清华大学等顶尖科研力量,深入解析肿瘤微环境特征,并提出了一系列免疫治疗增效新策略,将原本毫无免疫反应、被称为“冷肿瘤”的结直肠癌,转变为免疫细胞大量浸润的“热肿瘤”,让免疫系统重新“看见”并攻击癌细胞。这些发现,为无数对免疫药物耐药的患者重新打开了希望之门。在基础研究层面,团队揭示了直肠癌表观遗传新机制,通过泛素化、乙酰化及非编码RNA等,解释了肿瘤耐药和转移的深层原因,并为临床治疗提供精准治疗新靶点。
从“绝症”到“慢病”的转变
一名患者两年前因晚期结直肠癌伴肝转移被当地医院“劝退”,医生表示,肝脏全是转移灶。那时的她已经做好了最坏的打算。她辗转来到北京大学人民医院胃肠外科,MDT团队为她制定了“综合治疗+手术+靶向”的综合方案。团队通过精准评估,先通过新辅助治疗缩小肿瘤,再实施手术+肝脏射频消融,最后辅以个体化的靶向维持。
如今,患者体内的肿瘤已被完全控制,结肠肿瘤未再复发。像这样的故事不胜枚举。随着胃肠外科团队构建的早诊及治疗新靶点、免疫及遗传新机制、肿瘤精准治疗分子分型体系等研究成果的应用,越来越多的高危人群在早期就被筛查出来,避免疾病发展到晚期;越来越多的晚期患者,通过个体化诊疗得到康复,回归家庭和社会。
2026年荣获北京医学科技奖一等奖的成果,见证了北京大学人民医院胃肠外科团队用智慧与温情改写疾病定义的征程。随着这项成果在全国百余家医院推广应用,写入临床指南,并纳入国家行业标准,结直肠癌正逐步像高血压、糖尿病一样,成为一种可控、可管理的慢病。这不仅是技术的胜利,更是医学人文精神的回归——让每一个生命在尊严中延续,在希望中重生。

胃肠外科团队合影
(人民医院)
编辑:玉洁


